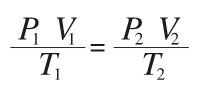Muy bien maestro le comparto la actividad completa exactamente como me la solicitan.
1. Lee el siguiente problema.
¿Por qué los alimentos se cuecen más rápido en una olla de presión?
En una olla normal con tapa, los alimentos reciben la presión atmosférica (1atm), y se logra una temperatura máxima de ebullición del agua, 100°C.
Para que el agua hierva a 100°C, el evento se realiza a nivel del mar (1 atm), si el experimento se llevara a cabo a una mayor altitud, tanto la presión atmosférica como el punto de ebullición disminuirían.
En una olla de presión, la presión que reciben los alimentos es mayor a la atmosférica (1 atm), a esta se agrega la presión por la acumulación de vapor de agua y el aumento en la temperatura de ebullición de 100°C. En un corto tiempo la presión total equivale a dos atmósferas (2 atm) y se mantiene constante debido a la válvula de seguridad que regula la salida de vapor cuando la presión sobrepasa cierto valor. Es por esto que se logra un cocimiento más rápido y por tanto un ahorro de energía.
La gráfica que relaciona la presión y la temperatura de una olla a presión no siempre es una recta, pero en la zona en que funciona normalmente podemos considerar que si lo es.
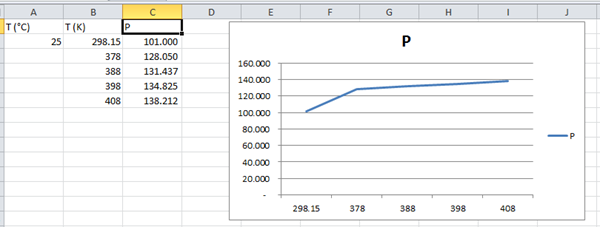
Al colocar un manómetro en una olla a presión, se obtuvo el siguiente resultado:
Temperatura (°C) = 25
Presión (Pa) = 101,000
2. Convierte T (°C) a K
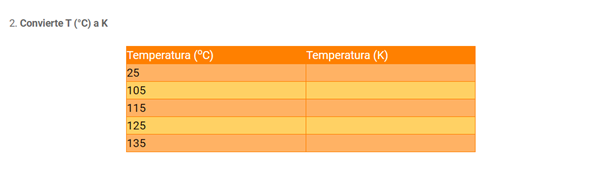
3. Calcula la Presión (Pa) en función de la temperatura en K
Temperatura (K) Presion (Pa)
298 = ?
378 = ?
388 = ?
398 = ?
408 = ?
4. Grafica los datos de la tabla del inciso 3.
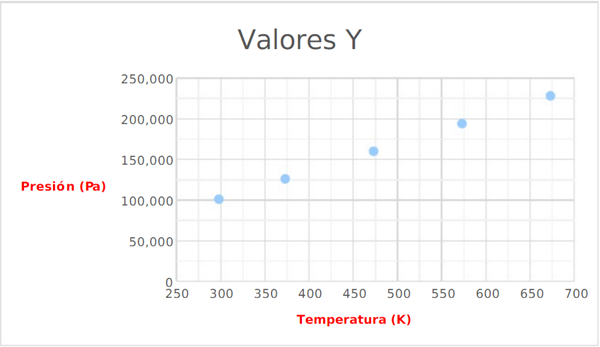
SOLO DE EJEMPLO NECESITA CORREGIRSE
5. El funcionamiento de olla de presión es proporcional entre estos valores de presión y temperatura, como el volumen de la olla no cambia, ¿qué ley se puede aplicar para entender su comportamiento? Explica brevemente tu respuesta.
6. Organiza la información y resultados en un archivo, recuerda incorporar el problema, los resultados de las tablas (incisos 2 y 3) con su procedimiento y solución; la gráfica con los resultados obtenidos, así como la pregunta y respuesta del punto 5.
Espero le sirvan los datos esta vez para poder resolverlo maestro Gustavo Omar Fellay
Le agradezco mucho de antemano
Saludos!